
CAS号:104987-11-3 | 分子式:C44H69NO12 | 制备方式:微生物发酵 | 生产菌株:筑波链霉菌
他克莫司是什么?
他克莫司是一种23元大环内酯类化合物,属于第二代免疫抑制剂,于1984年由日本藤泽制药公司从筑波链霉菌发酵培养物中首次发现[1]。他克莫司通过特异性结合钙调磷酸酶,抑制白细胞介素2(IL-2)合成,从而抑制T细胞活化,在器官移植术后抗排斥治疗中发挥重要作用[2]。与环孢素相比,他克莫司的免疫抑制效果是环孢素的10至100倍,且不良反应较少[3]。
核心技术参数
● 分子量:804.02
● 熔点:113-115°C
● 溶解性:易溶于DMSO、乙醇、丙酮,难溶于水
● 储存条件:-20°C密封保存
● 免疫抑制效力:比环孢素高10-100倍
物化性质
他克莫司为白色固体,CAS号是104987-11-3,分子式为C44H69NO12,从乙腈中结晶得到无色棱状结晶,熔点127-129°C,旋光度[α]D20为-84.4°(C=1.02,氯仿)。他克莫司易溶于甲醇、乙醇、丙酮、乙酸乙酯、氯仿或乙醚,难溶于己烷或石油醚,几乎不溶于水[2]。
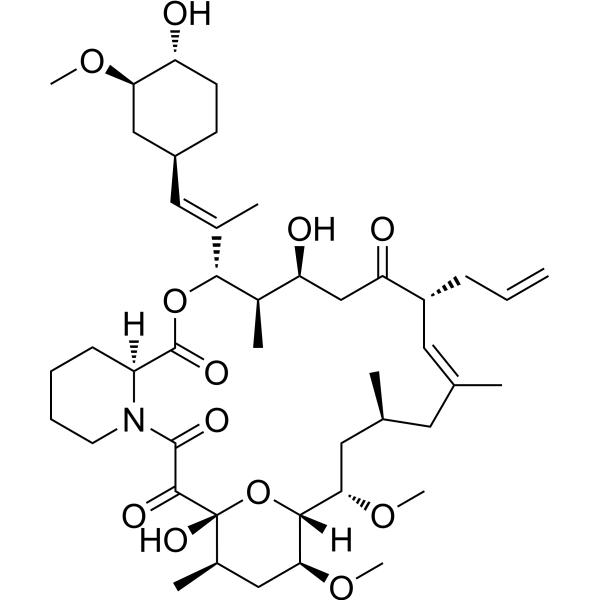 他克莫司化学结构式
他克莫司化学结构式
物理性质表
生物合成途径
他克莫司的生物合成途径复杂,由筑波链霉菌的fkb基因簇编码的I型聚酮合酶-非核糖体肽合成酶杂合系统合成。生物合成过程可分为4个部分:起始单元生成、聚酮链延伸、内酯环形成和后修饰[4]。起始单元(4R,5R)-4,5-二羟基环己-1-烯羧酸来自莽草酸途径;聚酮链由聚酮合酶FkbA、FkbB和FkbC催化延伸,需要2个丙二酰-CoA、5个甲基丙二酰-CoA、2个甲氧基丙二酰-ACP和1个烯丙基丙二酰-CoA作为延伸单元;内酯环由L-赖氨酸衍生的L-哌啶酸与聚酮链缩合形成;最后经过FkbM催化的C31羟基甲基化和FkbD催化的C9氧化两步修饰形成他克莫司[5]。
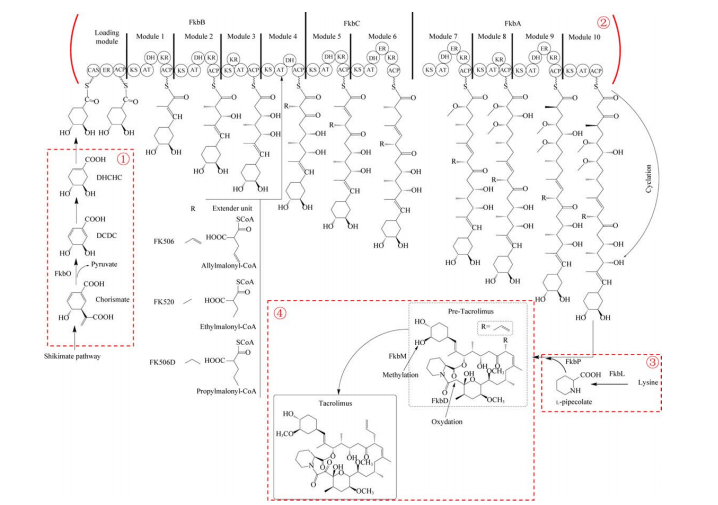 他克莫司生物合成途径一种
他克莫司生物合成途径一种
生物合成基因簇
他克莫司生物合成基因簇包含19-26个基因,核心基因包括fkbO(起始单元合成)、fkbABC(聚酮链延伸)、fkbGHIJK(甲氧基丙二酰-ACP合成)、allAKRD(烯丙基丙二酰-CoA合成)、fkbL(L-哌啶酸合成)、fkbP(成环)、fkbD和fkbM(后修饰)、fkbN和fkbR(调控)[6]。不同菌株中的基因簇结构存在差异,某些菌株含有额外基因如allMNPOS和tcs6-fkbR,但这些额外基因对他克莫司产量影响较小。
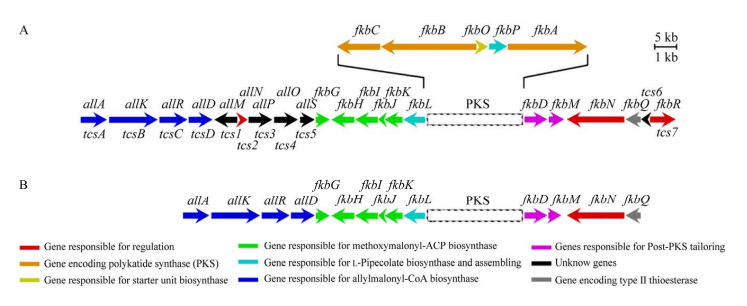 他克莫司生物合成基因簇
他克莫司生物合成基因簇
发酵制备方法
由于他克莫司分子量大、手性中心多、结构复杂,化学合成法效率较低,工业生产主要采用生物发酵法。筑波链霉菌No.9993是主要的他克莫司生产菌株。典型发酵工艺包括种子培养和主发酵两个阶段。种子培养基含甘油、玉米淀粉、葡萄糖、棉子粉、玉米浸渍液和碳酸钙,pH6.5,30℃培养4天。主发酵培养基含可溶性淀粉、玉米浸渍液、干酵母、碳酸钙和Adekancd,pH6.8,30℃发酵4天。发酵产物经硅藻土过滤、树脂吸附、乙酸乙酯提取、硅胶柱层析等多步纯化,最终得到白色结晶的他克莫司[2]。
发酵过程优化
为提高他克莫司产量,研究人员采用多种策略优化发酵过程。菌株选育方面,通过紫外诱变、NTG诱变、ARTP诱变等方法获得高产突变株。发酵工艺优化方面,采用响应面法优化培养基成分和培养条件。前体添加方面,补充莽草酸、赖氨酸、大豆油等前体物质显著提高产量。诱导剂方面,添加氯化镧、丁酸钠、DMSO、灭活酵母粉等诱导剂可大幅提升他克莫司产量。
产量提升案例
研发进展
他克莫司于1994年被美国FDA批准用于肝移植治疗,目前已广泛用于肾脏、肝脏和心脏同种异体移植术后的抗排斥治疗,也用于炎症性皮肤病等自身免疫性疾病[7]。
基因工程改造
为突破他克莫司生物合成瓶颈,研究人员开展基因工程改造研究。代谢途径改造方面,过表达fkbO、fkbL、fkbP、fkbD、fkbM等合成基因可提高产量10-40%,多基因共表达效果更显著[6]。调控基因改造方面,过表达fkbN(通路特异性正调控基因)可提高产量50-112%。前体供应强化方面,过表达pcc基因(丙酰-CoA羧化酶)和allAKRD基因(烯丙基丙二酰-CoA合成基因)可分别提高产量75.05%和149.84%。
代谢模型指导
基于基因组代谢模型的理性设计为代谢工程改造提供新思路。Huang等人建立了包含865个化学反应和621个代谢物的基因组代谢模型,预测并验证了dahp、pntAB、accA2等靶基因,过表达dahp基因使产量提高51.08%[8]。Wang等人结合静态优化方法和动态通量平衡分析优化模型,预测gcdh等靶基因,敲除gcdh使产量提高40.64%[1]。
适应症
他克莫司主要用于预防和治疗器官移植术后的急性排斥反应。在肾移植中,他克莫司已成为一线免疫抑制剂,KDIGO指南于2009年推荐将他克莫司作为初始和长期维持免疫抑制治疗用药[1]。在肝移植中,他克莫司可显著降低急性排斥反应发生率,提高移植物存活率。在心脏移植中,他克莫司同样表现出良好的抗排斥效果。除器官移植外,他克莫司还用于治疗特应性皮炎、银屑病等炎症性皮肤病[7]。
临床应用优势
与环孢素相比,他克莫司具有多方面优势:免疫抑制效果强10-100倍;急性排斥反应发生率低;移植物存活率高;不良反应较少,尤其是高血压、高血脂、多毛等副作用明显少于环孢素[3]。
药物监测
他克莫司口服吸收不完全且个体差异大,治疗窗窄,治疗剂量接近中毒剂量,因此必须监测血药浓度。他克莫司主要经肝脏CYP3A酶代谢,与多种药物存在相互作用。抗真菌药(酮康唑、氟康唑)、大环内酯类抗菌药(红霉素)等肝药酶抑制剂可升高血药浓度;利福平、糖皮质激素等肝药酶诱导剂可降低血药浓度[3]。中草药如五味子甲素、黄连素等也会影响他克莫司血药浓度,需避免同时服用。
应用领域
他克莫司在医学和科研领域有广泛应用。在临床医学中,他克莫司是器官移植抗排斥治疗的核心药物,每年挽救大量患者生命。在科研领域,他克莫司作为免疫抑制工具药,用于研究T细胞活化机制、免疫耐受诱导、自身免疫疾病发病机理等[1]。瀚香生物专注为科研机构和制药企业提供高质量的他克莫司产品和定制服务,支持免疫学、药理学和转化医学研究。
研究工具药
他克莫司是研究钙调磷酸酶信号通路的重要工具药。通过抑制钙调磷酸酶活性,他克莫司可阻断NFAT核转位,抑制IL-2等细胞因子表达,为研究T细胞活化提供可靠模型。在自身免疫疾病研究中,他克莫司用于建立疾病模型,评估治疗策略。在移植免疫研究中,他克莫司用于研究免疫耐受机制,探索新型免疫抑制剂。
药物开发
他克莫司的成功开发为免疫抑制剂研究提供重要参考。基于他克莫司的结构和作用机制,研究人员开发出多种衍生物和新型免疫抑制剂。
常见问题FAQ
Q:他克莫司和环孢素的区别是什么?
他克莫司和环孢素都属于钙调磷酸酶抑制剂,但存在多方面差异:作用机制上,他克莫司结合FKBP12,环孢素结合环孢素结合蛋白;免疫抑制效力上,他克莫司比环孢素强10-100倍;不良反应上,他克莫司的高血压、高血脂、多毛等副作用少于环孢素,但神经毒性、肾毒性略高;药代动力学上,他克莫司口服生物利用度较高,血药浓度个体差异大,需要更频繁的监测[3]。
Q:他克莫司的主要副作用有哪些?
他克莫司的主要副作用包括:肾毒性,表现为血肌酐升高、尿素氮异常;神经毒性,表现为震颤、头痛、失眠;糖代谢紊乱,表现为高血糖;感染风险增加,由于免疫抑制导致;胃肠道不适,表现为便秘、腹泻、恶心;其他不良反应包括高血钙、低血磷、白细胞减少、贫血等[1]。瀚香生物提醒用户,他克莫司仅供科研使用,不用于临床治疗。
Q:他克莫司如何保存?
他克莫司应在-20°C下密封保存,避免光照和潮湿。他克莫司在DMSO或乙醇溶液中于-20°C可保存长达2个月。配制好的溶液应分装后保存,避免反复冻融。
Q:他克莫司的治疗窗是什么?
他克莫司的治疗窗较窄,血药浓度范围因移植类型和检测方法而异。肾移植患者全血谷浓度通常为5-15ng/mL(检测方法:微粒子酶免分析法),肝移植患者为10-20ng/mL。浓度过低会增加排斥风险,浓度过高会增加肾毒性、神经毒性等副作用。瀚香生物强调,他克莫司仅供科研实验使用,不用于临床治疗,具体治疗方案需遵循临床医生指导[3]。
Q:他克莫司的生物合成菌株有哪些?
目前已报道超过15种可产生他克莫司的菌株,包括筑波链霉菌No.9993、筑波链霉菌L19、筑波链霉菌NRRL 18488、链霉菌KCTC 11604BP、卡那霉素链霉菌KCTC 9225、淡青链霉菌MTCC 5115等[5]。不同菌株的基因簇结构、产量水平和产物组成存在差异,需通过菌株选育、发酵优化和基因工程改造提高产量。
参考文献
[1] 金利群, 鲁笛, 邢明林, 等. 免疫抑制剂他克莫司生物合成的研究进展[J]. 生物工程学报, 2023, 39(8): 3095-3110.
[2] Kino T, Hatanaka H, Hashimoto M, et al. FK-506, a novel immunosuppressant isolated from a Streptomyces. I. Fermentation, isolation, and physico-chemical and biological characteristics[J]. The Journal of Antibiotics, 1987, 40(9): 1249-1255.
[3] Pirsch JD, Miller J, Deierhoi MH, et al. A comparison of tacrolimus (fk506) and cyclosporine for immunosuppression after cadaveric renal transplantation[J]. Transplantation, 1997, 63(7): 977-983.
[4] Motamedi H, Shafiee A, Cai SJ, et al. Characterization of methyltransferase and hydroxylase genes involved in the biosynthesis of the immunosuppressants FK506 and FK520[J]. Journal of Bacteriology, 1996, 178(17): 5243-5248.
[5] Chen DD, Zhang Q, Zhang QL, et al. Improvement of FK506 production in Streptomyces tsukubaensis by genetic enhancement of the supply of unusual polyketide extender units[J]. Applied and Environmental Microbiology, 2012, 78(15): 5093-5103.
[6] Huang D, Xia M, Li S, et al. Enhancement of FK506 production by engineering secondary pathways of Streptomyces tsukubaensis and exogenous feeding strategies[J]. Journal of Industrial Microbiology and Biotechnology, 2013, 40(9): 1023-1037.
[7] Lin AN. Innovative use of topical calcineurin inhibitors[J]. Dermatologic Clinics, 2010, 28(3): 535-545.
[8] Huang D, Li S, Xia M, et al. Genome-scale metabolic network guided engineering of Streptomyces tsukubaensis for FK506 production improvement[J]. Microbial Cell Factories, 2013, 12(1): 1-18.
本文内容基于公开发表的科学研究数据,由瀚香生物收集整理,仅供科研人员参考与学术交流,不可用于个人用途。