
索托拉西布(sotorasib,商品名Lumakras),研发代号AMG510,是一种有效的KRAS G12C共价抑制剂,通过选择性靶向KRAS p.G12C突变体,在DNA、RNA或蛋白质水平上阻断肿瘤细胞信号传导[1]。美国FDA于2021年5月28日批准安进公司开发的AMG510用于治疗成人携带KRAS G12C基因突变的非小细胞肺癌,适用于之前至少接受过一种系统疗法但治疗无效的患者。
KRAS是人体内最常见的突变致癌基因之一,在约13%的肺癌患者、3%的结直肠癌患者和2%的其他实体瘤患者中可检测到KRAS G12C突变[2]。KRAS蛋白是一种小GTP酶,在细胞信号传导通路中发挥重要作用,调控细胞增殖、分化和存活。G12C突变指第12位的甘氨酸被半胱氨酸替代,导致KRAS蛋白持续活化,促进肿瘤细胞生长。索托拉西布通过与KRAS G12C突变体中的半胱氨酸残基形成不可逆共价键,将KRAS蛋白锁定在非活性状态,阻断其下游信号传导[3]。
近期研究显示,索托拉西布不仅对KRAS G12C有效,还是一种广谱RAS G12C抑制剂。研究表明,索托拉西布对NRAS G12C的抑制效力比对KRAS G12C高5倍,这对携带NRAS G12C突变的肿瘤患者具有重要意义[4]。这一发现扩大了索托拉西布的潜在应用范围。

物化性质与制备方法
索托拉西布的化学名为6-氟-7-(2-氟-6-羟基苯基)-(1M)-1-[4-甲基-2-(丙烷-2-基)吡啶-3-基]-4-[(2S)-2-甲基-4-(丙烯酰基)哌嗪-1-基]吡啶并[2,3-d]嘧啶-2(1H)-酮,CAS登记号为2296729-00-3。分子式为C30H30F2N6O3,分子量为560.58 g/mol[5]。化学结构含氟代苯基、吡啶和吡啶嘧啶骨架,可溶于DMSO、DMF等有机溶剂。
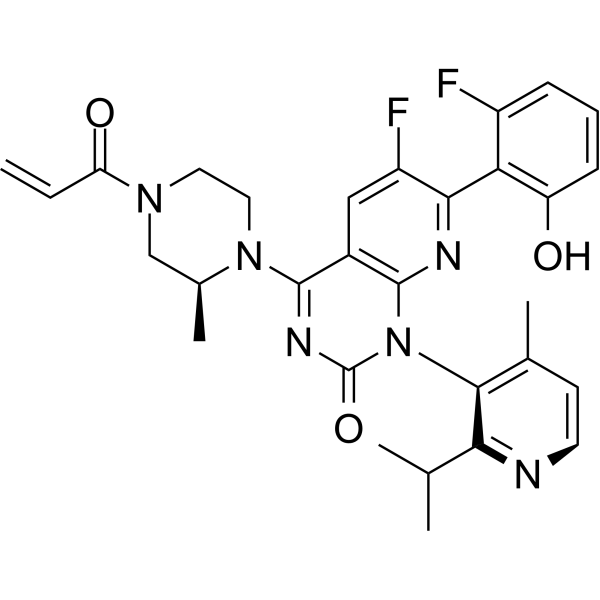 索托拉西布化学结构式
索托拉西布化学结构式
索托拉西布属于有机小分子化合物,其分子结构包含多个杂环系统:吡啶并嘧啶核心、吡啶环、哌嗪环和苯基取代基。这些结构特征赋予其良好的生物活性和代谢稳定性。氟原子的引入增强了分子的脂溶性和膜透过性,有利于其在体内的吸收和分布。
对于索托拉西布中间体的制备,药物技术领域报道了一种成熟的合成路线。该方法以苯乙酮为起始原料,在非质子性溶剂中与无机碱混合,升温搅拌均匀后分批加入2-氯乙胺盐酸盐,继续保温反应。反应完成后降温过滤,滤液减压浓缩得到油状化合物[6]。随后将油状化合物溶于水中,用盐酸调节pH至澄清,加入硫脲,升温蒸馏浓缩至内温达到108-110℃,继续回流反应。反应结束后降温结晶,过滤,滤饼用95%乙醇洗涤,干燥后得到中间体羟盐。该方法的羟盐收率可达90%以上,纯度可达99%以上,含量可达98%以上,工艺简单,适合工业化生产[6]。
索托拉西布的最终合成步骤涉及多个官能团的精细调控,包括酰胺键的形成、哌嗪环的构建以及丙烯酰基的引入。整个合成过程需要严格控制反应条件,包括温度、pH值、溶剂选择和反应时间,以确保产率和纯度。
作用机制研究
索托拉西布的作用机制基于其与KRAS G12C突变体的共价结合。KRAS G12C突变体在癌细胞内存在一种独特的变构结合位点,称为switch-II口袋。索托拉西布能够特异性识别并结合该口袋,与第12位的半胱氨酸残基形成不可逆的共价键[7]。这种共价结合将KRAS蛋白锁定在与GDP结合的非活性状态,阻止其与GTP结合和活化,从而阻断下游RAF-MEK-ERK信号通路,抑制肿瘤细胞增殖[8]。
值得注意的是,索托拉西布的选择性源于其对突变半胱氨酸的依赖。野生型KRAS蛋白在第12位是甘氨酸而非半胱氨酸,因此索托拉西布不会影响正常细胞中的野生型KRAS功能。这种突变选择性设计大大降低了药物对正常细胞的潜在毒性[9]。
结构生物学研究揭示了索托拉西布与KRAS G12C相互作用的分子细节。晶体结构显示,索托拉西布嵌入switch-II口袋,通过疏水相互作用和氢键网络稳定结合。其中,分子的异丙基吡啶基团与第95位组氨酸的疏水相互作用在结合稳定性中发挥重要作用[10]。
近期研究发现,RAS家族三个主要同工型(KRAS、NRAS、HRAS)的氨基酸序列高度相似。对多种KRAS G12C抑制剂的筛选表明,不同抑制剂对NRAS G12C和HRAS G12C的抑制活性存在显著差异[4]。索托拉西布对NRAS G12C的IC50比对KRAS G12C低5倍,显示其对NRAS G12C具有更强的抑制活性。这种差异主要归因于第95位氨基酸的不同:KRAS是组氨酸,NRAS是亮氨酸。结构分析和相互突变研究证实,亮氨酸95通过增强疏水相互作用,提高了索托拉西布与NRAS G12C的结合亲和力[4]。
研发历程与临床应用
索托拉西布的研发代表了针对"不可成药"靶点的成功案例。KRAS曾被认为是无法通过小分子药物靶向的难题,这一困境持续了近30年。2014年,安进公司与Carmot Therapeutics签订研究合作协议,利用Carmot的Chemotype Evolution技术平台进行先导化合物发现[11]。
索托拉西布的临床开发经历了快速推进。2018年启动I期剂量递增研究,2019年6月获得孤儿药资格认定,2020年12月获得突破性疗法认定,2021年2月获得优先审评资格,2021年5月28日获得加速批准上市[12]。这一快速获批路径反映了该药物在满足未满足医疗需求方面的重要价值。
CodeBreaK 100是索托拉西布的关键临床试验,包括I期剂量递增和II期注册研究。II期研究纳入了126例既往接受过至少一种系统治疗的KRAS G12C突变型晚期非小细胞肺癌患者,给予口服索托拉西布960 mg每日一次治疗[13]。中位随访12.2个月时,客观缓解率(ORR)为37%,疾病控制率(DCR)为81%,中位缓解持续时间(DOR)为10.0个月,中位无进展生存期(PFS)为6.8个月[13]。43%的缓解患者在数据截止时仍持续缓解无进展。
在结直肠癌患者中,索托拉西布也显示了一定活性。I期研究中纳入42例既往接受过至少两线系统治疗的KRAS G12C突变型转移性结直肠癌患者,客观缓解率为7%,疾病控制率为74%,中位无进展生存期为4.0个月[14]。
值得一提的是,近期临床报告显示,索托拉西布在NRAS G12C突变的结直肠癌患者中也显示出疗效。一例NRAS G12C突变的结直肠癌患者接受索托拉西布联合抗EGFR抗体帕尼单抗治疗后,获得了显著的肿瘤缓解[4]。这一临床案例证明了索托拉西布作为广谱RAS G12C抑制剂的实际应用价值。
安全性与注意事项
在临床研究中,索托拉西布显示出可管理的安全性特征。最常见的不良反应包括腹泻(42%)、肌肉骨骼疼痛(35%)、恶心(26%)、疲劳(26%)、肝毒性(25%)和咳嗽(20%)[15]。最常见的3级或4级不良事件包括肝毒性(12%)、丙氨酸氨基转移酶升高(11%)、天冬氨酸氨基转移酶升高(9%)、肌肉骨骼疼痛(8%)、肺炎(7%)和腹泻(5%)[15]。
严重不良事件发生率约50%,最常见的是肺炎(8%)、肝毒性(3%)和腹泻(2%)。因不良事件导致永久停药的患者比例为9%,主要原因是肝毒性(5%)。因不良事件需要减量的患者比例为5%,需要中断治疗的患者比例为34%[15]。
索托拉西布的药代动力学特征呈非线性和时间依赖性。在180-960 mg每日一次剂量范围内,稳态时系统暴露量相似。中位达峰时间约为1小时。稳态浓度在22天内达到,重复给药后无明显蓄积(平均蓄积比0.56)[16]。血浆蛋白结合率为89%,稳态分布容积为211 L[16]。
索托拉西布主要通过非酶促结合和CYP3A介导的氧化代谢进行生物转化。给药后74%的剂量随粪便排出(53%为原形药),6%随尿液排出(1%为原形药)。稳态时表观清除率为26.2 L/h,终末消除半衰期为5小时[16]。
常见问题FAQ
Q:索托拉西布对野生型KRAS有作用吗?
A:索托拉西布对野生型KRAS无抑制作用。其作用机制依赖于与突变半胱氨酸的共价结合,而野生型KRAS第12位是甘氨酸,不含半胱氨酸,因此索托拉西布不会影响正常细胞中的KRAS功能。
Q:索托拉西布也能抑制NRAS和HRAS的G12C突变吗?
A:可以。研究显示,索托拉西布对NRAS G12C的抑制效力比对KRAS G12C高5倍,对HRAS G12C也有相似活性。这使其成为广谱RAS G12C抑制剂,适用于携带NRAS或HRAS G12C突变的肿瘤。
Q:索托拉西布在什么条件下储存?
A:索托拉西布应在干燥、阴凉、避光条件下储存,通常建议在-20°C或以下长期保存,以保持其化学稳定性。具体储存条件可参考产品说明书。
Q:索托拉西布的主要不良反应有哪些?
A:最常见的不良反应包括腹泻、肌肉骨骼疼痛、恶心、疲劳、肝毒性和咳嗽。其中需要特别关注的是肝毒性,用药期间需要定期监测肝功能。
参考文献
[1] 夏训明编译.美国FDA批准首种治疗KRAS基因突变型非小细胞肺癌的靶向药物Lumakras(sotorasib)[J].广东药科大学学报,2021,37(3):1-3.
[2] Blair HA. Sotorasib: First Approval[J]. Drugs,2021,81(11):1573-1579.
[3] Canon J, Rex K, Saiki AY, et al. The clinical KRAS(G12C) inhibitor AMG 510 drives anti-tumour immunity[J]. Nature,2019,575(7781):217-223.
[4] Rubinson DA, Tanaka N, Fece de la Cruz F, et al. Sotorasib Is a Pan-RAS G12C Inhibitor Capable of Driving Clinical Response in NRAS G12C Cancers[J]. Cancer Discovery,2024,14(5):727-736.
[5] Amgen Inc. LUMAKRAS(sotorasib) tablets, for oral use: US prescribing information[Z]. 2021.
[6] 张浩波,浦坤峰,宋雪剑.一种Sotorasib中间体的制备方法:中国,202110786392[P]. 2021.
[7] Lanman BA, Chen JJ, Liu L, et al. Discovery of AMG 510, a first-in-human covalent inhibitor of KRAS G12C for the treatment of solid tumors[J]. Cancer Research,2019,79(13 Suppl):4455.
[8] Saiki AY, Gaida K, Rex K, et al. Discovery and in vitro characterization of AMG 510-a potent and selective covalent small molecule inhibitor of KRAS G12C[J]. Cancer Research,2019,79(13 Suppl):4484.
[9] Hong DS, Fakih MG, Strickler JH, et al. KRAS G12C inhibition with sotorasib in advanced solid tumors[J]. New England Journal of Medicine,2020,383(13):1207-1217.
[10] Skoulidis F, Li BT, Govindan R, et al. Overall survival and exploratory subgroup analyses from the phase 2 CodeBreaK 100 trial evaluating sotorasib in pretreated KRAS p.G12C mutated non-small cell lung cancer[J]. Journal of Clinical Oncology,2021,39(15 Suppl):460s.
[11] Carmot Therapeutics. Carmot Therapeutics enters into drug discovery collaboration with Amgen[EB/OL]. 2014-01-14.
[12] US Food & Drug Administration. FDA grants accelerated approval to sotorasib for KRAS G12C mutated NSCLC[EB/OL]. 2021-05-28.
[13] Li B, Skoulidis F, Falchook G, et al. Registrational phase 2 trial of sotorasib in KRAS p.G12C mutant NSCLC: first disclosure of the Codebreak 100 primary analysis[J]. Journal of Thoracic Oncology,2021,16(3 Suppl):S61.
[14] J?nne PA, Ou SHI, Cho BC, et al. Phase 2 study of sotorasib in KRAS G12C-mutated advanced colorectal cancer[J]. Annals of Oncology,2021,32(S5):S581-S582.
[15] Spira A, Wilson FH, Shapiro G, et al. Patient-reported outcomes (PRO) from the phase 2 CodeBreaK 100 trial evaluating sotorasib in KRAS p.G12C mutated non-small cell lung cancer (NSCLC)[J]. Journal of Clinical Oncology,2021,39(15 Suppl):474s.
[16] Cardona P, Simiens M, Purkis J, et al. An open-label study to evaluate the effect of omeprazole on the pharmacokinetics of sotorasib (AMG 510) in healthy subjects[J]. Clinical Pharmacology & Therapeutics,2021,109(Suppl 1):S31.
本文内容基于公开发表的科学研究数据,由瀚香生物收集整理,仅供科研人员参考与学术交流,不可用于个人用途。