
在药物研发的历史长河中,很少有药物能够像依伐卡托(Ivacaftor, CAS: 873054-44-5)这样,从分子机制到临床应用都展现出清晰的科学逻辑。作为首个针对囊性纤维化(Cystic Fibrosis, CF)病因而非症状的药物,依伐卡托不仅改变了一种罕见病的治疗格局,更为精准医疗时代提供了典型范例。
依伐卡托的化学名称为N-(2,4-二叔丁基-5-羟基苯基)-1,4-二氢-4-氧代-3-喹啉甲酰胺,分子式为C24H28N2O3,分子量为392.49。从外观上看,依伐卡托呈现为白色至类白色固体粉末,熔点范围在212-215°C之间,沸点约为550.4°C(预测值),密度为1.187 g/cm3。

依伐卡托化学结构式
在溶解性方面,依伐卡托表现出典型的疏水性特征。它在DMSO中具有良好的溶解性(约78 mg/mL),但在水和乙醇中几乎不溶。这种溶解特性决定了其在药物制剂中的给药方式。储存条件要求较为严格,需要在**-20°C下避光防潮密闭保存**,以保持其化学稳定性。
从结构上看,依伐卡托包含一个关键的喹啉酮骨架,这是药物化学中重要的药效团,广泛存在于多种生物活性化合物和重磅药物中。分子中的酰胺键作为连接"优势构建模块"和二叔丁基苯酚的关键纽带,在药用化学中具有多重作用:既可通过氢键与结合位点相互作用,又因其代谢不稳定性为药物代谢提供了可调控位点。
依伐卡托的研发历程堪称现代药物发现的教科书案例。囊性纤维化是一种常染色体隐性遗传疾病,由CFTR(囊性纤维化跨膜传导调节因子)基因突变引起,导致患者多个器官功能逐渐衰退,严重威胁生命。在全球约7万名CF患者中,约95%的病例由CFTR基因突变导致,但不同突变类型对治疗的响应存在显著差异。
美国Vertex制药公司的研究团队确立了明确的研发目标:开发一种可口服的小分子药物,通过恢复变异CFTR通道功能来达到治疗效果。筛选和评价化合物活性的方法基于两种互补机制:一是增强功能,即化合物通过促进CFTR离子通道开启的概率来增加离子流动;二是纠正功能,即改善缺失Phe508的CFTR的加工和向细胞表面的传输。
研发团队对228,000个化合物进行了高通量筛选,最终发现了苗头化合物,其EC50为2.1 μmol/L。进一步的分子解析表明,该化合物是通道蛋白的促进剂而非CFTR功能的激活剂。这一发现为后续的结构优化指明了方向。
通过对喹啉酮和胺片段的系统性结构优化,研究团队合成了约70多个化合物,系统研究了构效关系。关键发现包括:去除并合苯环会失去活性,提示该片段需要一定的亲脂性;N1上的氢原子至关重要,推测其作为氢键给体参与结合作用。
依伐卡托的合成涉及多个步骤,主要围绕两个关键中间体的构建和偶联展开。Vertex公司在专利文献中详细描述了多条合成路线,其中最具代表性的是采用Gould-Jacobs反应合成喹啉酮片段。
在最初的合成路线中,喹啉酮通过三步收敛路线合成,而苯胺片段则通过四步反应获得。关键的连接步骤采用HATU(六氟磷酸O-(7-氮杂苯并三唑-1-基)-N,N,N',N'-四甲基脲鎓)作为偶联试剂,在DMF中进行酰胺键形成反应,最终以71%的收率得到依伐卡托。
在改进的第二代路线中,研究团队用T3P(丙烷膦酸酐)替代HATU作为偶联剂,这一改变带来多项优势:T3P在相对温和的条件下展现出高效性,减少了副反应或不需要副产物的风险;它与广泛的官能团兼容,适合多种底物;此外,T3P是结晶固体,便于处理和储存。
中国研究机构也开发了具有自主知识产权的合成路线,如上海工程技术大学和Laurus Pharma独立开发了相似的方法,分别以邻硝基苯甲酸和邻氟苯甲酸为起始原料。这些替代路线为依伐卡托的工业化生产提供了多样化选择。
值得关注的是,科研人员还开发了基于Witkop-Winterfeldt氧化的合成方法,通过臭氧氧化将吲哚基团转化为喹啉,展现了有机合成方法学的创新应用。

依伐卡托合成路线
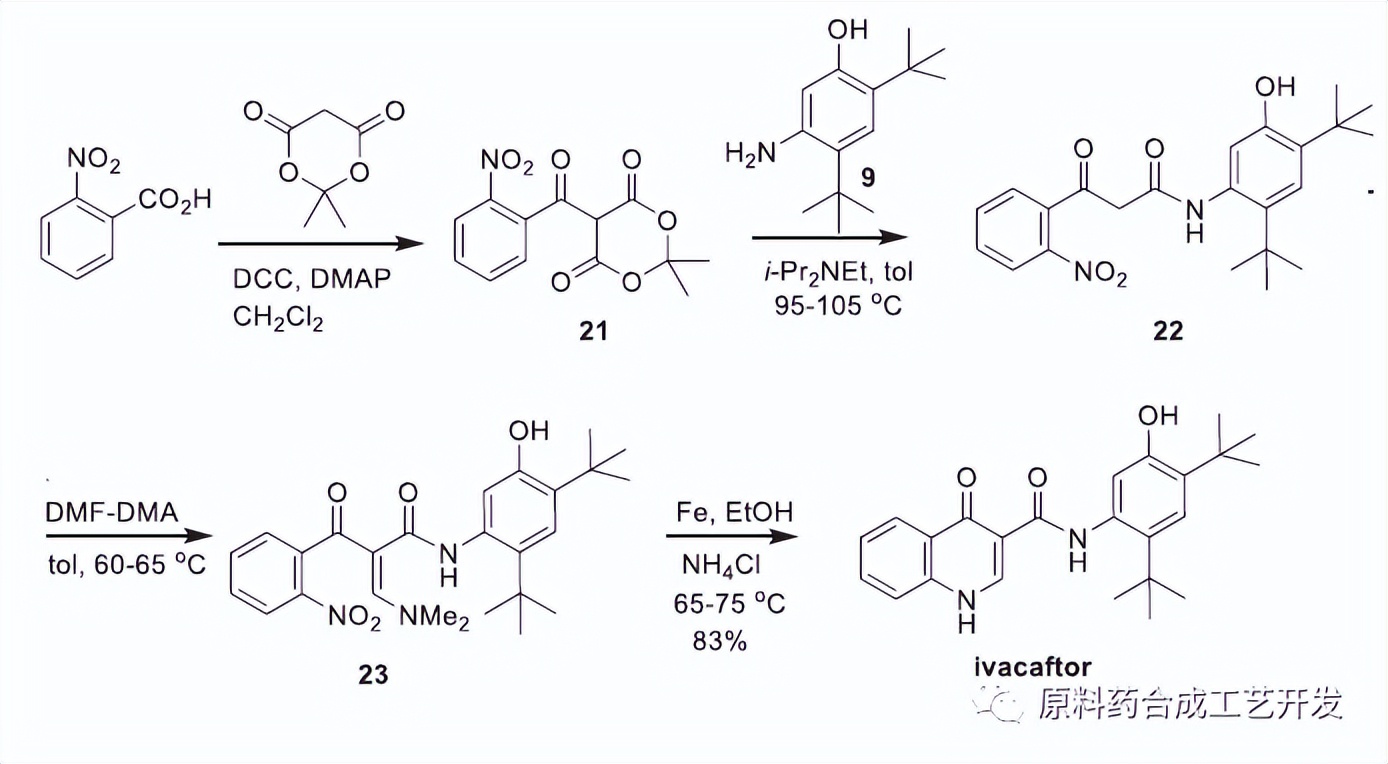
依伐卡托SNAr反应路线合成
依伐卡托作为CFTR增强剂(Potentiator),其作用机制已通过多项研究得到阐明。CFTR蛋白是一种在多种器官上皮细胞顶端质膜表达的阴离子通道,受蛋白激酶A调控,负责氯离子和碳酸氢根离子的转运。
在CF患者中,CFTR基因的突变导致蛋白功能异常。其中,G551D突变是典型的III类门控突变,甘氨酸在551位被天冬氨酸取代,导致CFTR蛋白虽然能够到达细胞表面,但通道开放概率显著降低。依伐卡托通过直接与CFTR通道结合,诱导非传统的门控模式,显著提高通道开放概率。
研究数据显示,依伐卡托(10 μM)可使G551D-CFTR、F508del-CFTR和野生型CFTR的开放概率分别提高约6倍、5倍和2倍。在表达G551D突变的Fisher大鼠甲状腺细胞中,依伐卡托显著提高毛喉素刺激的氯离子分泌,EC50为100 nM;在表达F508del突变的重组细胞中,EC50为25 nM。
更令人印象深刻的是,在携带G551D和F508del CFTR突变型的原代培养人CF支气管上皮细胞中,依伐卡托有效提高毛喉素刺激的氯离子分泌,提高幅度达10倍,EC50为236 nM,有效性比常用的CFTR增强剂染料木素高70多倍。
依伐卡托于2012年1月获得美国FDA批准,商品名为Kalydeco,用于治疗6岁及以上携带特定CFTR基因突变的患者。主要适应症包括G551D突变(占CF病例的4-5%)以及其他多种突变类型。
临床试验结果令人振奋。在成人患者研究中,治疗48周后,依伐卡托组患者的肺功能(FEV1)平均绝对值提升10.4%,而安慰剂组下降0.2%。儿童患者(6-11岁)的结果更为显著,FEV1平均绝对值提升达12.5%。
除肺功能改善外,依伐卡托治疗还带来了多方面的临床获益:肺部恶化事件减少约一半,静脉抗生素使用频率降低,住院率下降;成人患者呼吸相关生活质量评分显著提高;儿童患者体重增长加速;汗液氯化物浓度显著下降,这是疾病严重程度的关键指标。
依伐卡托更大的价值体现在组合疗法中。与CFTR校正剂(Corrector)联合使用,可显著扩大适用患者人群。目前批准的组合疗法包括:
鲁玛卡托/依伐卡托(Lumacaftor/Ivacaftor,商品名Orkambi):用于携带两个F508del突变拷贝的患者,2015年获FDA批准。
替扎卡托/依伐卡托(Tezacaftor/Ivacaftor,商品名Symdeko/Symkevi):用于携带F508del突变的患者,2018年获批。
依来卡托/替扎卡托/依伐卡托(
Elexacaftor/Tezacaftor/Ivacaftor,商品名Trikafta/Kaftrio):这是目前最有效的CFTR调节疗法,适用于携带至少一个F508del突变或对治疗有响应的其他突变的患者,覆盖约90%的CF人群。该三联疗法于2019年获FDA批准,是囊性纤维化治疗的重要里程碑。
在Trikafta组合中,依来卡托和替扎卡托帮助更多CFTR蛋白到达细胞表面,依伐卡托则增强CFTR蛋白在细胞表面的开放概率。三者协同作用,使更多功能正常的CFTR蛋白出现在细胞表面,显著改善氯离子转运,稀释黏液分泌物。
临床数据显示,在携带一个F508del突变和另一种突变的患者中,治疗24周后,ppFEV1平均提高13.9个百分点;在携带两个F508del突变拷贝的患者中,ppFEV1平均提高10.4个百分点。瀚香生物观察到,这种多药联合策略代表了罕见病治疗的重要发展方向。
依伐卡托口服吸收良好,但水溶性低(<0.05 μg/mL)。与高脂食物同服可显著改善吸收,AUC增加2.5倍,达峰时间从3小时延迟至5小时。血浆蛋白结合率约为99%,主要与α1-酸性糖蛋白和白蛋白结合。
依伐卡托在人体内被广泛代谢,主要通过CYP3A酶系(包括CYP3A4和CYP3A5)。主要的两个代谢产物为M1(羟甲基依伐卡托)和M6(依伐卡托羧酸酯),其中M1具有约为依伐卡托1/6的活性,被认为是药理活性代谢物;M6活性低于依伐卡托的1/50,不被认为具有药理活性。
口服给药后,大部分依伐卡托(87.8%)在代谢转化后通过粪便排出,M1和M6两个主要代谢产物占总消除剂量的约65%(其中M1占22%,M6占43%)。尿中原形药物排泄可忽略不计。在进食状态下单次给药后,表观终末半衰期约为12小时。
由于依伐卡托主要通过CYP3A代谢,与影响该酶活性的药物联用时需特别注意:
强CYP3A诱导剂(如利福平、圣约翰草)可能显著降低依伐卡托血药浓度,导致疗效减弱,应避免联用。
与强CYP3A抑制剂(如酮康唑)联用时,剂量需减至150 mg每周2次;与中度CYP3A抑制剂(如氟康唑)联用时,剂量减至150 mg每日1次。
依伐卡托的耐受性总体良好。最常见的不良反应(发生率≥5%)包括头痛(17%)、上呼吸道感染(16%)、鼻塞(16%)、恶心(10%)和皮疹(10%),多为轻至中度且短暂。
需要关注的严重风险包括肝功能异常(ALT/AST升高),建议在治疗前及第一年每3个月监测一次肝酶,之后每年一次;儿童患者需进行基线及随访眼科检查,因有非先天性晶状体混浊的报告。
依伐卡托的生产涉及复杂的化工和制药产业链。上游原料主要包括2,4-二叔丁基苯酚、邻硝基苯甲酸或邻氟苯甲酸、二乙基乙氧基亚甲基丙二酸酯等化工原料,以及各类保护基试剂、偶联剂等。
中间体生产是产业链的关键环节。4-氧代-1,4-二氢喹啉-3-羧酸和5-氨基-2,4-二叔丁基苯酚(或其碳酸酯保护衍生物)是两个核心中间体,其质量直接影响最终产品的纯度和收率。
原料药生产需要严格的质量控制和工艺优化。全球有多家企业具备依伐卡托原料药生产能力,包括中国的多家制药企业。原料药的合成工艺需要平衡收率、成本和质量要求,同时满足环保和安全生产标准。
制剂生产方面,依伐卡托可制成片剂或颗粒剂。片剂为薄膜包衣片,需与含脂肪食物同服以提高生物利用度。制剂工艺需解决依伐卡托低水溶性带来的溶出和吸收问题。
依伐卡托的成功催生了多种衍生物和类似物的研发。其中,针对依伐卡托代谢转化位点设计的氘代物显示出良好前景,具有延长半衰期和降低用药频度的潜力,体现了电子等排置换在药物优化中的应用价值。
在组合疗法领域,基于依伐卡托的双联和三联药物已成为CF治疗的标准方案。Trikafta/Kaftrio作为目前最有效的CFTR调节疗法,其成功经验正在向其他单基因罕见病领域推广。
未来研究方向包括:开发适用于更广泛突变类型的CFTR调节剂;降低药物成本,提高可及性;探索新生儿和婴幼儿早期干预的治疗策略;以及开发更安全的替代疗法。
Q1: 依伐卡托适用于所有囊性纤维化患者吗?
A: 不是。依伐卡托仅适用于携带特定CFTR基因突变的患者,主要包括G551D、R117H等突变类型。用药前需通过FDA批准的CF突变检测确认突变类型。对于携带F508del突变的患者,需使用包含校正剂的组合疗法。
Q2: 依伐卡托能治愈囊性纤维化吗?
A: 不能。依伐卡托是针对CF病因的治疗药物,可显著改善患者症状和生活质量,延缓疾病进展,但不能根治疾病。患者需要长期服药以维持疗效。
Q3: 为什么依伐卡托需要与含脂肪的食物同服?
A: 依伐卡托水溶性低,与高脂食物同服可显著提高其生物利用度,AUC可增加2.5倍。这有助于确保药物达到有效血药浓度。
Q4: 依伐卡托有哪些主要药物相互作用需要注意?
A: 主要是与CYP3A酶相关的相互作用。应避免与强CYP3A诱导剂(如利福平)联用,与强或中度CYP3A抑制剂联用时需调整剂量。
Q5: 使用依伐卡托需要定期监测哪些指标?
A: 主要包括肝功能(ALT、AST等),治疗前及第一年每3个月监测一次,之后每年一次。儿童患者还需定期眼科检查。此外应监测呼吸功能(FEV1)、体重、汗液氯化物等疗效指标。
Van Goor F, Hadida S, Grootenhuis PDJ, et al. Rescue of CF airway epithelial cell function in vitro by a CFTR potentiator, VX-770. Proc Natl Acad Sci U S A. 2009;106(44):18825-18830.
Hadida S, Van Goor F, Grootenhuis PDJ, et al. Discovery of N-(2,4-di-tert-butyl-5-hydroxyphenyl)-4-oxo-1,4-dihydroquinoline-3-carboxamide (VX-770, ivacaftor), a potent and orally bioavailable CFTR potentiator. J Med Chem. 2014;57(23):9776-9795.
Ramsey BW, Davies J, McElvaney NG, et al. A CFTR potentiator, ivacaftor, provides clinical benefit for CF patients with G551D mutation. N Engl J Med. 2011;365(18):1663-1672.
Middleton PG, Mall MA, Drevinek P, et al. Elexacaftor-Tezacaftor-Ivacaftor for Cystic Fibrosis with a Single Phe508del Allele. N Engl J Med. 2019;381(19):1809-1819.
Liu F, Zhang Z, Levit A, et al. Structural identification of a hotspot on CFTR for potentiation. Science. 2019;364(6446):1184-1188.
郭宗儒. 囊性纤维化治疗药依伐卡托的研制. 药学学报. 2020;55(11):2746-2750.
本文内容基于公开发表的科学研究数据,由瀚香生物收集整理,仅供科研人员参考与学术交流,不可用于个人用途。